Choroby autoimmunologiczne w zespole Downa cz.2 przyczyny deficytów immunologicznych w zespole Downa
marzec 4, 2014 by Jarek
Kategoria: Wiedza o Zespole Downa
W momencie gdy czytamy opracowania naukowe na temat chorób autoimmunologicznych w zespole Downa, przyczyny leżą z jednej strony w genetyce z drugiej strony w deficytach mikroelementów typowych dla zespołu Downa, a wynikających z błędnych procesów metabolicznych. Z kolei, gdy chcemy poznać te mechanizmy lepiej wszystkie drogi z powrotem prowadzą do genetyki i systemu obrony immunologicznej organizmu.
Definicje jakie się pojawią w tym wpisie pochodzą z wikipedia.org
W tej części tego wpisu chciałbym przyjrzeć się raportom, które analizowały ten problem. Zakończę ich analizę moim podsumowaniem.
IMMUNOLOGIA
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3074212/
W raporcie tym analizuje się problem stałych infekcji i braku odporności w ZD. Za główne przyczyny w tej kwestii wskazuje się zredukowaną ilość limfocytów typu T i B, brak ekspansji normalnych limfocytów w dzieciństwie, stąd dzieci z ZD do około 5 roku życia chorują zdecydowanie częściej niż dzieci bez ZD.
http://www.nature.com/pr/journal/v67/n5/full/pr2010102a.html
Limfocyty T inaczej limfocyty grasicozależne (T od łac. thymus – grasica) – komórki układu odpornościowego należące do limfocytów odpowiedzialne za komórkową odpowiedź odpornościową. Komórki prekursorowe, nie posiadające cech limfocytów T, wytwarzane są w czerwonym szpiku kostnym, następnie dojrzewają głównie w grasicy, skąd migrują do krwi obwodowej oraz narządów limfatycznych
Limfocyty B, inaczej limfocyty szpikozależne (B od łac. Bursa Fabricii – kaletka Fabrycjusza) – komórki układu odpornościowego należące do limfocytów odpowiedzialne za humoralną odpowiedź odpornościową, czyli wytwarzanie przeciwciał. Limfocyty B powstają w szpiku kostnym, a w przebiegu odpowiedzi immunologicznej różnicują się w obwodowych narządach limfatycznych w komórki plazmatyczne i komórki pamięci
Innymi czynnikami negatywnie wpływającymi na układ odpornościowy to brak odpowiedniej reakcji na szczepienia, obniżona odpowiedź immunologiczna IgA, spadek hemostazy neutrofilów jak i zredukowana ilość młodych komórek T. W zakresie anatomicznym wskazuje się na zdecydowanie mniejszą wielkość grasicy, która pełni istotną rolę w rozwoju odporności organizmu.
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2759463/
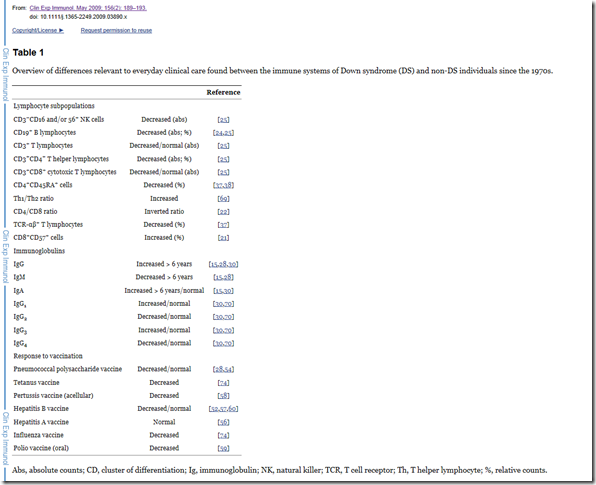
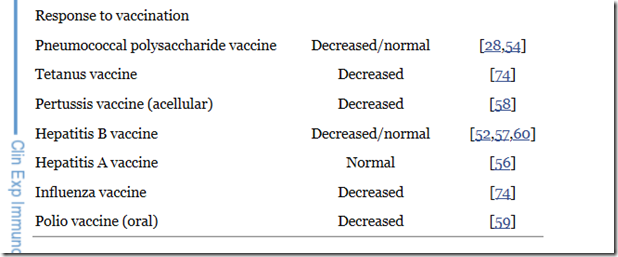
Jak analizuje się w powyższym raporcie reakcja immunologiczna i “fenomen” chorób autoimmunologicznych w ZD, obrazowany jest od wielu lat w postępowaniu klinicznym i rejestruje się znaczące jego odchylenia. Ciekawym wątkiem jest tutaj podkreślenie, że osoby z ZD dużo gorzej reagują na konkretne szczepienia, przez co bariera immunologiczna nie poprawia się jak to ma miejsce u grupy kontrolnej.
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2759463/table/tbl1/
Obniżona odpowiedź na szczepienia w ZD:
A tutaj tak pisałem o tych szczepieniach:
http://www.zespoldowna.info/zespol-downa-i-szczepienia-cz-4-szczepienia-a-odpornosc.html
Zostawiając już temat objawów defektów immunologicznych należy przyjrzeć się wskazaniom genetycznym w tym obszarze.
SOD 1, RCAN 1 od zawsze kandydaci numer 1
http://www.ncbi.nlm.nih.gov/m/pubmed/23644448/
http://www.ncbi.nlm.nih.gov/m/pubmed/24505143/
Rola RCAN 1 w zespole Downa od zawsze była przedmiotem rozważań. Przypomnę, że jeszcze do niedawna gen RCAN 1 nazywany był DSCR 1 co oznacza Krytyczny Region Zespołu Downa 1. Nazwa podkreślała jego istotność. Jak widać na załączonych diagramach, RCAN będąc w istotnej nadekspresji przekraczającej jako gen 185% standardowej aktywności, powoduje w systemie immunologicznym spadek pierwotnej reakcji immunologicznej oraz zaburza funkcjonowanie limfocytów typu T.Zauważcie, że obniża tzw. reakcję zapalną jak i odpowiedź organizmu na alergię czy wstrząs anafilaktyczny.
W przypadku SOD 1, który jest odpowiedzialny za reakcję na aktywność wolnych rodników, to on nie radzi sobie z ich liczbą. Prowadzi to do trwałego uszkodzenia mózgu poprzez stan zapalny. System immunologiczny nie radzi sobie z wolnymi rodnikami i poziom różnorodnych antyutleniaczy w organizmie osoby z ZD jest zbyt niski, by z nierównowagą w tym zakresie sobie umiał poradzić.
http://www.bioline.org.br/pdf?hg04016
The gene encoding copper-zinc superoxide
dismutase (SOD-I) is located on chromosome 21 and
enzymatic activity shows a gene dosage effect leading
to 150% activity in DS individuals. It is speculated that
increased SOD-I leads to low levels of superoxide anions
and reduced destruction of organisms which require
superoxide radicals for efficient killing. Low serum zinc
levels have also been proposed as a possible reason
for impaired chemotaxis observed in DS individuals,
since that mineral has a role in promoting chemotaxis
as well as being a cofactor in T-cell responsiveness.
Dyskutuje się przy tym o potencjalnej roli niedoborów cynku, który jednoznacznie jest wiązany z SOD.
http://www.zespoldowna.info/antyutleniacze-w-zespole-downa-troche-historii-cz-2.html
http://www.zespoldowna.info/antyutleniacze-w-zespole-downa-cz-3.html
Inni kandydaci w “parach” to gen CBS i IL-2. Nadekspresja genu CBS prowadzi do nadmiernej produkcji H2S. W efekcie prowadzi to do zmian w funkcjonowaniu genu IL-2 i spadku bariery immunologicznej.
http://www.sciencedirect.com/science/article/pii/S1110863013000372
Inną kwestią jest rola genów związanych z chorobą Alzheimera w destrukcyjnym procesie obniżania barier immunologicznych. Zarówno APP, S100B jak i znów RCAN 1 odgrywają przemożną rolę w tym procesie. Choroba Alzheimera w istocie jest to proces dotyczący mechanizmów obronnych, gdyż zarówno amyloid, jak i cynk pełniące istotną rolę w procesie obrony organizmu, w konsekwencji stają się częścią patologicznych amyloidów beta, które są toksyczne i niszczące dla każdej komórki.
http://www.zespoldowna.info/zlogi-amyloidowe-i-app.html
Jak wejdziemy na poniższy link otworzy nam się tabelka.
http://www.dingdown.com.br/site/pdf/publicacoes/public/RPViewDoc.pdf
Porównuje ona liczbę genów wpływających na pracę limfocytów. Ta część po prawej jest dla osoby z ZD, ta po lewej dla normalnego limfocyta. Największa ilość genów wiąże się z obszarem immunologii i reakcji immunologicznej. Mnie to już dzisiaj nie dziwi.
MIKRO RNA
Nie wiem dlaczego, ale tak jestesmy przyzwyczajeni do naszych genów typu APP, DYRK 1 A, RCAN 1 czy SOD, że zapominamy o istnieniu innych genów. W ZD jest gen, który nazywa się MIR 155 i okazuje się, że ma przemożny wpływ na odpowiedź immunologiczną, choroby autoimmunologiczne.
miRNA (mikroRNA) – jednoniciowe cząsteczki RNA o długości ok. 21-23 nukleotydów, regulujące ekspresję innych genów. miRNA kodowane są przez genom komórki, jak normalne geny, i transkrybowane przez RNA polimerazę II, tak samo, jak mRNA. Prekursorem są niewielkie RNA, o strukturze spinki do włosów, które ulegają obróbce podobnie do siRNA. Wchodzą w skład kompleksów rybonukleoproteinowych blokujących specyficznie translację mRNA i nadają im specyficzność. W odróżnieniu od siRNA, miRNA nie posiadają 100%-owej identyczności sekwencji do docelowego mRNA. miRNA są zaangażowane w negatywną regulację ekspresji genów podczas rozwoju; ocenia sie, ze biorą udział w regulacji 30% ludzkich genów. Są mediatorami mechanizmu interferencji z translacją mRNA (RNAi).
http://www.ncbi.nlm.nih.gov/m/pubmed/23246696/
W jednym z ostatnich raportów na jego temat z grudnia 2013 roku, pojawia się zdanie:
“…miR-155-5p plays a critical role in various physiological and pathological processes such as hematopoietic lineage differentiation, immunity, inflammation, viral infections, cancer, cardiovascular disease, and Down syndrome. In this review we summarize the mechanisms by which MIR155 expression can be regulated”.
czyli MIR 155-5p odgrywa kluczową rolę w różnych fizjologicznych i patologicznych procesach, takich jak podział krwiotwórczych komórek macierzystych, odporności, stanach zapalnych, przy infekcjach wirusowych, w przypadku raka, chorób serca (kardiologicznych) oraz w przypadku zespołu Downa. W tym raporcie podsumowaliśmy mechanizmy dzięki którym ekspresja MIR 155 może być regulowana.
MOJE PODSUMOWANIE:
Deficyty odporności w ZD są wielowymiarowe. Na początku są geny. Potem defekty autonomiczne jak grasica. W następnym etapie mamy problemy z limfocytami, ilością, dojrzałością. Skutkuje to bardzo słabą odpornością do wieku 5 lat. Oznacza to, że proces immunosupresji jest zakodowany i oznaczony na pierwsze 5 lat życia osoby z ZD. Nie jest to jednak wszystko. Na koniec życia, u osób z ZD pojawiają się symptomy degeneracji barier immunologicznych wywołane rozwojem patogennych objawów charakterystycznych dla choroby Alzheimera.
Z perspektywy obecnego stanu wiedzy, kluczowe są geny zarządzające mRNA. Jest ich 5, ale w istocie to ten jeden MIR 155 determinuje uruchamianie procesów chorobowych. Jest on początkiem, gdy inne geny przejmują rozwój danego stanu dokładając swoją część negatywnych aktywności. Zatem to MIR 155 powinien w tym obszarze stać się naszym celem terapeutycznym. Jest to możliwe, ale o tym już jutro.