Udar i choroba moyamoya w zespole Downa.
listopad 23, 2017 by Jarek
Kategoria: Mózg, układ nerwowy
Nie ma badań w kierunku udarów w zespole Downa. Jest bardzo mało opracowań naukowych w tym kierunku, a jak się okazuje ich pojawienie się jest równie częste jak celiakii w ZD. Dlaczego nikt tym się nie zajmuje? Udary występują albo w wieku do 3-4 roku życia, albo gdy osoba z ZD jest już dorosła i nikt tego po prostu nie łączy. W ZD występują 26 razy częściej niż u osób bez…a mimo wszystko nie jest to badane.
Największą grupą badań objęto dzieci do lat 3, gdzie udar ma typologię zespołu nazwanego moyamoya, a cechą charakterystyczną jest krwotok śródmózgowy. U dorosłych choć w ponad 30% wiąże się udar z wadami serca i układu krwionośnego, to w istocie nie ma precyzyjnej informacji o charakterystyce przebiegu tego procesu, który wtedy jest obarczony dużym ryzykiem śmierci.
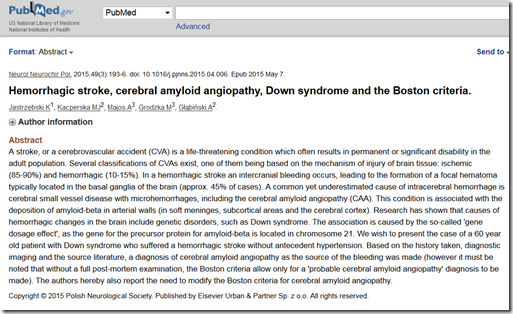
Obraz cyfrowej angiografii subtrakcyjnej prawej tętnicy środkowej mózgu u pacjenta z chorobą moyamoya
https://pl.wikipedia.org/wiki/Choroba_moyamoya#/media/File:Moyamoya02.jpg
W tych nielicznych badaniach jakie się pojawiają na ten temat powielają się następujące sformułowania opisujące ten stan: “Ryzyko udaru niedokrwiennego w DS wydaje się głównie zależeć od ryzyka sercowo-zatorowego.Większe ryzyko udaru krwotocznego i mniejsze ryzyko zdarzeń wieńcowych (u mężczyzn) w ZD pozostaje niewyjaśnione.”
Zatem jesteśmy w sytuacji, gdy nikt nic nie wie, a i sam problem nie jest precyzyjnie badany ze względu na jego etiologię.
http://www.jns-journal.com/article/S0022-510X(17)30110-7/fulltext
Rozpoczniemy zatem w inny sposób naszą analizę. Najczęściej występujący typ udaru krwotocznego u małych dzieci nazywa się moyamoya. Cechami charakterystycznymi występowania tego zespołu są:
-miażdżyca
-anemia sierpowata
i zespół Downa.
https://pl.wikipedia.org/wiki/Choroba_moyamoya
“Podstawą rozpoznania jest obraz angiograficzny mózgu, gdyż widoczne są na nim licznie rozwijające się naczynia krążenia obocznego, tworzące charakterystyczne dla tej choroby „kłęby dymu”.”
“U dzieci występują porażenie połowicze, ból głowy, zawroty głowy, drgawki, ruchy mimowolne, upośledzenie umysłowe”
U dorosłych może to być element patologii choroby Alzheimera, choć z mojej perspektywy nikt tego dokładnie nigdy nie analizował…a dla mnie jest to ten element, który u każdego z chorobą Alzheimera się pojawia i u osób z ZD tak samo. Przecież choroba Alzheimera to choroba o podłożu cholesterolowym i dysfunkcji objawowej układu krwionośnego. Tzw, otępienie naczyniowe jest powodem demencji po udarowej w chorobie Alzheimera. Dla mnie ten mechanizm, który dotyka każdego w inny sposób i w innym czasie, w zespole Downa może dzięki ekspresji genów z 21 chromosomu być problemem już od urodzenia dziecka….ale to później.
https://www.alzheimers.org.uk/info/20007/types_of_dementia/5/vascular_dementia
http://www.alzforum.org/news/research-news/small-brain-bleeds-lead-bigger-problems-alzheimers
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4075149/
https://www.sciencedaily.com/releases/2016/06/160613122335.htm
https://f1000.com/prime/ext/726346694
https://www.ncbi.nlm.nih.gov/pubmed/20925005
https://www.ncbi.nlm.nih.gov/pubmed/26048609
Z perspektywy badań nad chorobą Alzheimera kandydatem może to być gen APOE4 na allelach rs7412 oraz rs429358, który jest głównym mechanizmem pojawiania się tego typu problemu.
http://www.zespoldowna.info/ktory-apoe-jest-ryzykiem-choroby-alzheimera.html
Innym częstym wariantem jest gen NOTCH3 zlokalizowany na chromosomie 19q12 . Najrzadziej występującym wariantem jest gen COL4A1-A2.
W najnowszych badaniach nad tym problemem pojawiają się następujące geny:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5338082/
-PON1 w dwóch wariantach Q192R i L55M oba “powszechnie” występujące w panelach naszych dzieci
http://www.zespoldowna.info/pon1-i-mthfr.html
-TNF-α, który pojawia się niemal w każdej dysfunkcji w ZD
-MTHFR C677T, który jest też powszechnie występującym polimorfizmem u naszych dzieci i u nas samych
oraz
-TGF-β1, MACROD2, FOXF2, TSPAN2, ALDH2,ABCA7,CLU.
http://onlinelibrary.wiley.com/doi/10.1111/1440-1681.12558/pdf
Wróćmy jednak do problemów z udarem u dzieci. Głównym “winowajcą “są geny HLA, MTHFR C677T, ACTA-2. Jeżeli popatrzymy na poziom celiakii w ZD to dla mnie ten gen jest kandydatem numer 1 w ZD obok MTHFR.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4502238/table/T1/
http://www.zespoldowna.info/hla-dqa1-i-hla-drb1-to-geny-ktore-wplywaja-na-poziom-iq-w-zd.html
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4502238/
Inną grupą genów są polimorfizmy na poziomie genów RNF 213.
Wiemy zatem, że udary w ZD są niejako kolejnym zaburzeniem łączącym ZD, chorobę Alzheimera i polimorfizmy rodzicielskie. Jak sobie z tym radzić?
PROTOKOŁY SZPITALNE.
Interwencja neurochirurgiczna jest najczęściej stosowanym protokołem leczniczym w połączeniu z podawaniem aspiryny w dawce 3 mg/kg/dzień.
http://austinpublishinggroup.com/pediatrics/download.php?file=fulltext/ajp-v2-id1017.pdf
http://casereports.bmj.com/content/2017/bcr-2017-219894.abstract
http://thejns.org/doi/pdf/10.3171/2014.12.PEDS14563
PROTOKOŁY SUPLEMENTACYJNE.
Popatrzmy na to co już wiemy. Geny genami, a działania objawowe mogą być korygowane. Tak pisałem o korygowaniu działania genu PON1:
“… w przypadku genu PON 1 wskazana jest suplementacja witaminą C, E, EGCG, DHA, resveratrolem, oliwą z oliwek, kurkumą, kwercytyną, glutationami które zwiększają jego aktywność. Należy pamiętać przy tym, że aktywność tego genu jest najmniejsza w wieku 0-3 by później istotnie rosnąć. Oznacza to, że przy polimorfizmach MTHFR u dzieci wyżej wymienione suplementy poprawiające funkcjonowanie genu PON 1 powinny być podawane w większych dawkach w tym wieku 0-3 niż później.”
Z perspektywy samych naczyń krwionośnych i pojawiania się wysokiego ciśnienia przed udarowego należy przyjmować NAD i l-argininę, są to dla mnie te same mechanizmy jakie występują w przypadku wysokiego ciśnienia w ciąży. Objawowo mogą być leczone w ten sam sposób. Widać to zresztą przy opisach leczenia aspiryną u bardzo małych dzieci w tym kierunku.
Z mojej perspektywy jeżeli tak na to popatrzymy podstawowy protokół powinien wyglądać zatem w ten sposób dla osoby w wieku ok. 18 lat:
-l-arginina 4 000 mg
-l-citrulina 200 mg
-regulacja metylacji via kwas foliowy (MTHFR)
-antyutleniacze ze szczególnym uwzględnieniem witaminy C
http://www.ashg.org/genetics/ashg07s/f10318.htm
Pozostaje pytanie na koniec: czy powinniśmy to podawać wszystkim dzieciom od urodzenia?
Zarówno citrulina jak i arginina mogą być istotnym wsparciem dla mitochondriów w ZD. Protokoły metylacyjne mamy już w swoim portfolio. Jeżeli badania genetyczne byłyby robione powszechnie wtedy też można by adresować protokoły w sposób personalny uwzględniając ścieżki metaboliczne obarczone największym błędem. Dla mnie tutaj jest szczególna rola NAD.
W sytuacji jednak, gdy nie mam jednak tych analiz, jednoznacznie bym uwzględniał od początku życia dzieci z ZD, pełny ten protokół ze szczególną uwagą u dzieci, których matki miały wysokie ciśnienie w trakcie ciąży. Może być to pomocne wielowymiarowo.