Witamina B12.
listopad 8, 2019 by Jarek
Kategoria: Suplementy, leki i ich kontrola
Wydaje mi się, że odpowiadałem na to pytanie już wielokrotnie, ale jeżeli jest to wciąż trudne to powtórzę się.
Po pierwsze suplementowanie witaminą C w dużych ilościach może upośledzić absorpcję witaminy B12.
Po drugie geny, środowisko, jelita. Poniżej wszystko opisane, tylko skorzystać.
Wchłanianie witaminy B12 jako problem, w naszym kraju dzieli się na dwie populacyjne subgrupy: tych z “rodzinną historią” z przedwojennej Polski wschodniej i tej z Polski zachodniej. Ci pierwsi systemowo tak bym to ujął mają większy problem z utrzymanie witaminy B12 w organizmie, tytułem różnych problemów, gdy Ci drudzy mają jedynie problemy dietetyczne, by w sposób zbilansowany dostarczać witaminę B12 z cynkiem.
Zaczynamy jednak od genów i wskazań na co i dlaczego powinniśmy popatrzeć w pierwszej kolejności.
http://www.zespoldowna.info/polimorfizmy-zwiazane-z-witamina-b12.html
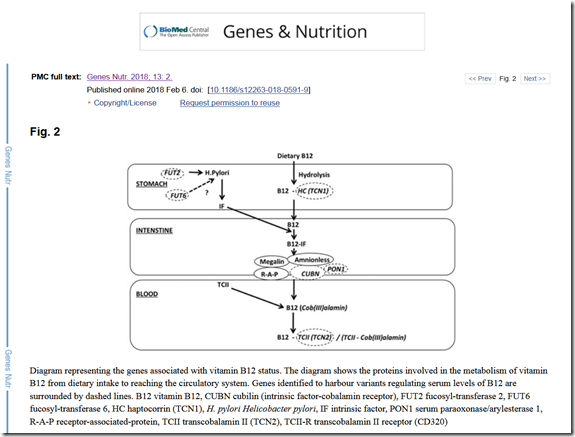
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5801754/figure/Fig2/
Do tej pory dyskutowaliśmy głównie o metylacji, ale skoro pojawiają się pytania, to musimy sięgnąć głębiej do pobierania witaminy B12 z żywności. Ma to miejsce w układzie pokarmowym począwszy od żołądka po jelito grube.
Witamina B12 produkowana jest głównie przez bakterie żyjące w układzie pokarmowym zwierząt. U człowieka powstaje w symbiozie z bakteriami układu pokarmowego. Następuje to dopiero w dystalnych częściach układu trawiennego, to jest w jelicie grubym. Ma to znaczące konsekwencje, gdyż w tej części jelit witaminy nie podlegają wchłanianiu i wszystko co wyprodukują bakterie, zostaje wydalone wraz z kałem.
Witamina B12 występuje głównie w produktach pochodzenia zwierzęcego. Do źródeł witaminy B12 w pożywieniu człowieka należą produkty mięsne, ryby, jajka, mleko i jego przetwory, pieczarki[4]. W witaminę tę często są wzbogacane płatki śniadaniowe[5]. Wbrew wcześniejszym poglądom, glony nie zawierają witaminy B12, tylko jej analog strukturalny, który w przypadku człowieka jest nieprzyswajalny i może utrudniać wchłanianie właściwej witaminy. Produkty sojowe są wzbogacane w witaminę B12 w celu zapobiegania niedoborom tej witaminy u osób, które nie spożywają produktów odzwierzęcych (weganie). Stosuje się także suplementy diety. Pewne wskazówki może zawierać również dieta Genmai-Saishoku, która zawiera brązowy ryż, warzywa oraz algi morskie. Jest to dieta wegańska, jednak poziom witaminy B12 w osoczu dorosłych i dzieci, którzy ją stosują, nie odbiega od wyników grupy kontrolnej[6]. Jak dotąd naukowcom nie udało się wytłumaczyć tego zjawiska[7].
https://pl.wikipedia.org/wiki/Witamina_B12
Kluczowe geny/mechanizmy w tym procesie to:
-FUT2, FUT6 na ich pracę ma wpływ Helicobacter pylori
-TCN 1 jako haptokoryna
-IF czyli czynnik Castle’a, za który odpowiada gen CUBN
https://pl.wikipedia.org/wiki/Czynnik_wewn%C4%99trzny
-PON 1 gen występujący powszechnie w polimorfizmie w Polsce
http://www.zespoldowna.info/pon1-i-mthfr.html
-TCN 2
-CD 320 receptor witaminy B12 na ścieżce TCN2
http://www.zespoldowna.info/polimorfizmy-zwiazane-z-witamina-b12.html
-MTR w metylacji
-MTRR w regeneracji witaminy B12 w metylacji
Są one jednoznacznie wiązane z metylacją i jej jakością.
W kontekście mitochondriów, tak istotnych w ZD, pojawiają się następujące geny:
-ABCD 4
-LMBRD1
-CLYBL
-DNMT2
-MS4A3
-PRELID2
-MMAA I MMAB
-MMADHC
-MUT
Wszystkie powyższe geny mają wpływ na metabolizm witaminy B12 w organizmie, jednakże większość z nas definiuje swoje braki przede wszystkim w oparciu o geny związane z metylacją i do tego wrócimy.
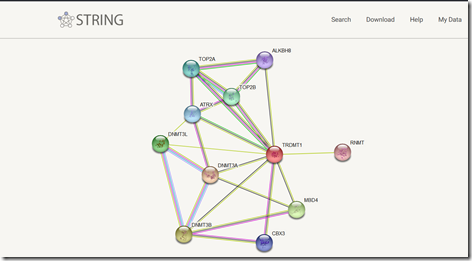
Zacznę od jednego. Pojawia się w tym zestawie gen o nazwie DNMT2 (TRDMT1) , który podlega funkcjonalnemu połączeniu z genem DNMT3L, który jest potrojony w ZD. Nie ma badan w kierunku ZD, ale zmiana wartości ekspresji genu DNMT2 pod wpływem tego drugiego może wpływać negatywnie na jego działanie. Oznacza to, że aktywność DNMT3L może wpływać w sposób swoisty na poziom funkcjonowania witaminy B12 w ZD.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4112773/
https://journals.plos.org/plosgenetics/article?id=10.1371/journal.pgen.1003530
Druga kwestia. Brak odpowiedniego wchłaniania witaminy B12 jest aż w ponad 50% dziedziczna. Co to znaczy? Specyficzne polimorfizmy dziedziczone pokoleniowo mają wpływ na określony wzór absorpcji witaminy B12.
Przechodzimy teraz do miejsc krytycznych.
ŻOŁĄDEK
W ramach tej części układu trawiennego mamy kilka punktów krytycznych związanych z absorpcją witaminy B12. Podstawowa jest związana z funkcjonowaniem haptokoryny czyli funkcjonowaniem genu TCN1 (rs526934, rs34528912, rs34324219), która wiąże się z witaminą B12. Chroni dietetyczną witaminę B12 przed kwaśnym środowiskiem żołądka. Jej polimorfizm po prostu osłabia tą aktywność.
Geny FUT2 i FUT6 są genami w istocie związanymi z funkcjonowaniem Helicobacter pylori. FUT 2 bierze udział w syntezie antygenów z układu Lewisa, pośrednicząc w przyłączaniu patogenów żołądka (patrz H.pylori) do błony śluzowej żołądka, co może wpływać na wchłanianie witaminy B12, jej ograniczenie. FUT6 wspiera tą aktywność. W efekcie, gdy występują określone polimorfizmy powyższych genów i infekcja H.pylori, następuje istotny brak wchłaniana witaminy B12 na zasadzie blokowania tego procesu.
Polimorfizmy FUT2 wpływające na absorpcję B12 rs281379, rs492602, rs516316, rs601338, rs602662, rs838133,rs1047781.
Uważa się, że “allel "A" SNP rs602662 jest związany ze stanem nieseptycznym (antygeny H null), co może zmniejszyć ryzyko infekcji bakteryjnej przez patogeny, takie jak H. pylori, oraz wyjaśnia, dlaczego osoby z allelem "A" mają wysoki poziom witaminy B12”.
https://pl.wikipedia.org/wiki/Uk%C5%82ad_grupowy_Lewis
Nie jest to częsty przypadek, ale złe funkcjonowanie czynnika Castle’a może całkowicie zablokować wchłanianie witaminy B12. Ilość tego czynnika jest w istotnym stopniu zależna od występowania patogenów takich jak H. pylori.
Obie ścieżki zależą od prawidłowego działania genu PON1, który odpowiedzialny jest za prawidłową detekcję infekcji bakteryjnej. Jego polimorfizm oznacza, osłabienie jego aktywności i brak reakcji organizmu na problem patogenów. Jeżeli mamy polimorfizmy FUT2, sprzyjające wzroście patogenów (rs492602, rs601338), to powinniśmy się spodziewać dużo niższego poziomu witaminy B12, gdy w innych przypadkach wysokiego poziomu witaminy B12 a w szczególności gdy mamy polimorfizm rs602662.
Ten stan dotyczy także jelit, gdzie czynnik Castle’a wciąż działa pozwalając na absorpcję i transport “dietetycznej” witaminy B12. Na ten transport wpływają geny takie jak: ABCD4, LMBRD1. Kluczowym jest także proces wychwytu witaminy B12 i związania jej z endocytami. Za to odpowiedzialny jest gen CD320 i jego polimorfizm powodujący redukcję wychwytu witaminy B12.
Wszystkie powyższe mechanizmy są zmienne tytułem wystąpienia stanów zapalnych w tym odcinku układu trawiennego, infekcji bakteryjnych, dysbiozy i leczenia tych stanów. Witamina B12 bez dobrych bakterii nie powstanie (Lactobacillus spp., Propionibacterium spp., Bifidobacterium spp.), a te procesy modyfikują, obniżają ich liczbę!!!
https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0107232
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4260394/
https://onlinelibrary.wiley.com/doi/full/10.1111/j.1365-2672.2011.05157.x
LECZENIE:
Oczywiście należy korygować objawy, budować odpowiednią mikrobiotę, likwidować stan zapalny…ale gdy brakuje witaminy B12 to konieczne są iniekcje z hydroksykobalaminy.
KREW
Błędy metylacyjne najczęściej kojarzymy ze statusem witaminy B12 we krwi. Przypomnę, że badanie serum witaminy B12 jest jednym z najmniej precyzyjnych badań diagnostycznych…stąd powinniśmy ją badać w przypadku istotnych problemów jako holo-TC, czyli poziom witaminy B12 w postaci aktywnej. Odpowiedzialny za transport witaminy B12 na tym etapie jest gen TCN2, ściśle związany z występowaniem także choroby Alzheimera.
rs1801198 genu TCN2 w układzie homozygotycznym jest układem o istotnym, mniejszym poziomie dostępności witaminy B12 we krwi. Błąd w jego funkcjonowaniu prowadzi po prostu do “nierozpoznawania” witaminy B12 przez co mniejszego poziomu jej transportu.
http://www.zespoldowna.info/polimorfizmy-zwiazane-z-witamina-b12.html
https://www.snpedia.com/index.php/Rs1805087
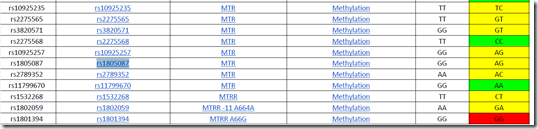
Gen MTRR i jego allela A66G rs1801394 jest odpowiedzialna za utrzymywanie odpowiedniej ilości aktywnej witaminy B12 w postaci metylokobalaminy i jest najczęściej badana w tym kierunku. Jednakże ostatnie badania wskazują na istotną rolę innych polimorfizmów regulujących poziom witaminy B12 w postaci: rs162036, rs162048, rs1532268 i rs3776455, których nie znajdziemy w panelach, albo nie występują populacyjnie w Polsce.
Nie można pominąć tutaj funkcjonowania genu MTR z kluczowym polimorfizmem rs1805087. Przy czym ten polimorfizm nie jest związany z wychwytem, a wykorzystaniem witaminy B12. Polimorfizm przyspieszony powoduje istotne braki witaminy B12 i zdecydowaną deregulację funkcjonowania metylacji gdy współtowarzyszy temu polimorfizm genu MTHFR C677T.
LECZENIE:
Doustnie witamina B12 w postaci metylokobalaminy/hydroksykobalaminy o ile nie towarzyszą temu problemy opisane powyżej.
MITOCHONDRIA
Pierwszy gen MMAA uczestniczy w translokacji witaminy B12 do mitochondriów, ponadto MMAA może odgrywać ważną rolę w ochronie i reaktywacji mutacji metylmalonylo-koA (MCM).
Drugi gen to MUT. Dostarcza instrukcji do tworzenia mutacji metylmalonylo-CoA (MUT), która jest enzymem mitochondrialnym. “MUT działa jak katalizator, który izomeryzuje metylmalonylo-CoA do sukcynylo-CoA [91]. MUT wymaga 5-prime-deoksyadenozylokobalaminy (AdoCbl), która jest formą B12, która działa z MUT, tworząc sukcynylo-CoA. Sukcynylo-CoA uczestniczy w cyklu TCA (cykl trikarboksylowy) w celu uzyskania energii [92]. Gen MUT bierze udział w metabolizmie homocysteiny i zależy od jego funkcji [93]. Cztery badania donoszą o związkach między wariantami w obrębie genu MUT.”
Genem, który odgrywa w tym procesie także istotną rolę jest gen MMAB, który uczestniczy w formowaniu adenosylokobalaminy, kofaktora do produkcji energii w ramach cyklu TCA (cykl Krebsa)
http://www.zespoldowna.info/jak-wspierac-mitochondria-w-zespole-downa.html
http://www.zespoldowna.info/zdrowe-mitochondria-moga-zatrzymac-rozwoj-choroby-alzheimera.html
LECZENIE:
Iniekcje z hydroksykobalaminy, podawanie adenosylokobalaminy.




Super wpis. Dziekuję że się dzielisz wiedzą.